Для кого: широкая аудитория, нутрициологи, специалисты по функциональному и интегративному подходу к здоровью.
Тип доказательств: обзор современных данных PubMed (обсервационные исследования, когортные анализы, генетические работы, клинические случаи) с комментариями и интерпретацией с позиций доказательной и функциональной медицины.
Дадали Чат
Консультации по нутрициологии на базе знаний профессора Дадали
Получите научно-обоснованные рекомендации в чате, где работают как живые специалисты, так
и интеллектуальный бот, обученный на лекциях профессора Владимира Абдулаевича Дадали
Главное из статьи за 30 секунд
- Синдром Жильбера — это не просто «безобидная генетическая особенность», а состояние, при котором печень хуже справляется с билирубином, и это отражается в анализах при любой дополнительной нагрузке.
- Генетический дефект в гене UGT1A1 создаёт сниженный «запас прочности» фермента, но запускают синдром модифицируемые факторы: голодание, стресс, лекарственная нагрузка, вирусные инфекции.
- Стандартный генетический тест проверяет только один из более чем 100 вариантов гена — «отрицательный» результат не исключает синдром; при этом сам по себе результат проверки одного гена не означает, что синдром будет проявляться.
- Ген изменить невозможно, но снизить нагрузку от триггеров — вполне реальная задача, которая и даёт практический результат.
- Умеренно повышенный билирубин обладает антиоксидантными и кардиопротективными свойствами — но это не повод игнорировать триггеры.
- Главный лекарственный риск — иринотекан; также важна осторожность со статинами, атазанавиром и длительным ежедневным приёмом парацетамола.
Что такое Синдром Жильбера простыми словами
Синдром Жильбера — это состояние, при котором в крови периодически (или постоянно) повышается уровень непрямого (несвязанного) билирубина. В основе лежит снижение активности печёночного фермента UGT1A1 (уридин-дифосфат-глюкуронозилтрансфераза 1А1) — именно он «упаковывает» токсичный непрямой билирубин в водорастворимую форму, безопасно выводимую с желчью.
Когда фермент работает вполсилы, а нагрузка на систему нормальная — человек может годами не знать о своём синдроме. Но как только нагрузка возрастает — вирусная инфекция, голодание, лекарства, стресс — система перестаёт справляться, и билирубин выходит за пределы нормы.
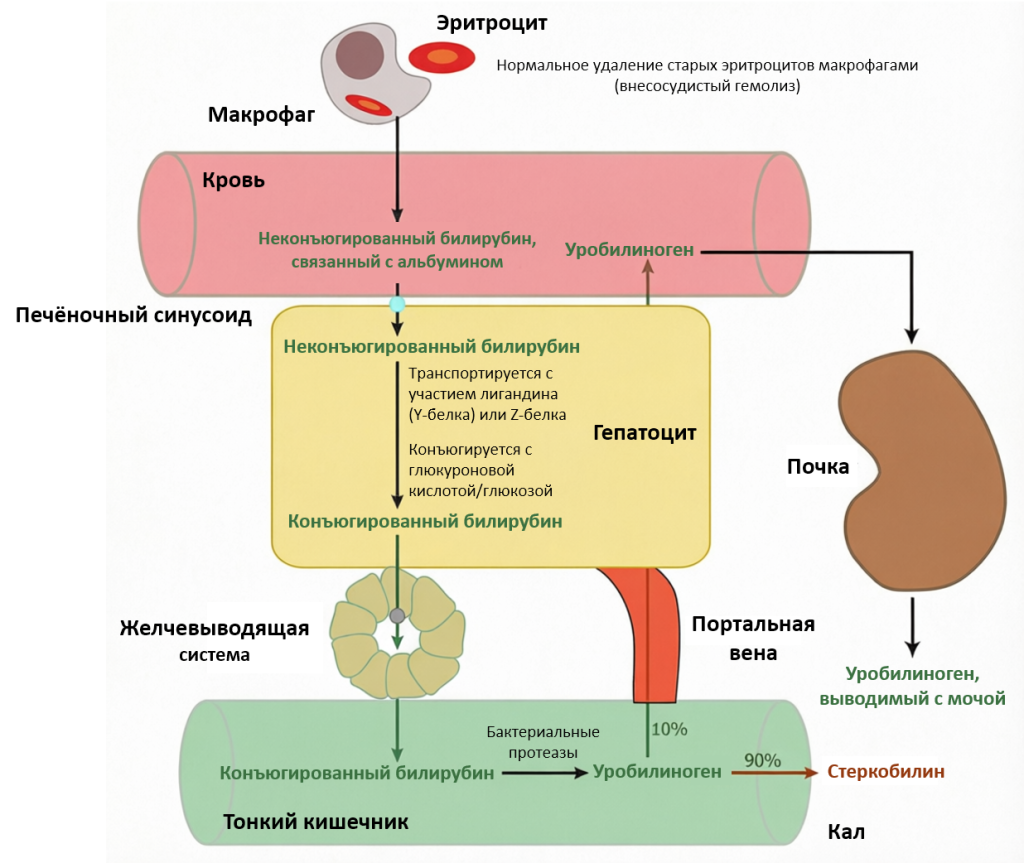
Синдром Жильбера — что за болезнь простыми словами? Важная оговорка прямо в названии: это именно синдром, а не болезнь. Синдром — устойчивый комплекс признаков и изменений в анализах, связанных общим механизмом, но не отдельное заболевание с собственным течением и стандартом лечения. Речь идёт о генетически обусловленном состоянии с особым типом обмена билирубина, которое проявляется только при определённой нагрузке, а не о прогрессирующей патологии печени.
Распространённость синдрома
Частота носительства генетического варианта UGT1A1*28 в европейской популяции — 8–10% в гомозиготной форме (оба гена изменены), ещё 30–40% людей являются гетерозиготными носителями. С учётом всех генетических вариантов (а их более 100) реальная распространённость составляет от 5 до 20% в зависимости от этнической принадлежности и диагностических критериев.
При этом значительная часть носителей никогда не попадает в поле зрения врача: синдром проявляется только при сочетании генетической предрасположенности и активных триггеров. Иными словами, реальное число людей, у которых синдром есть, но не диагностирован, значительно выше официальной статистики.
Синдром Жильбера у мужчин встречается и клинически проявляется значительно чаще, чем у женщин: соотношение в разных исследованиях — от 2:1 до 7:1. Причина — андрогены подавляют активность UGT1A1, а у мужчин выше исходная скорость оборота гемоглобина. Типичный дебют — пубертатный период, когда тестостерон начинает ингибировать фермент.
Синдром Жильбера у женщин проявляется мягче, но специфически связан с гормональными колебаниями: усиление желтушности во время менструации, при беременности, на фоне оральных контрацептивов. Нередко диагноз впервые выставляется при плановых анализах во время беременности.
Осложнения при синдроме Жильбера
Сам по себе синдром не вызывает прогрессирующего поражения печени и цирроза. Однако называть его «полностью безобидным» — значит недооценивать реальную картину:
- Лекарственная токсичность — главный реальный риск. Ряд препаратов, метаболизируемых UGT1A1, при сниженной активности фермента накапливается в организме до токсических концентраций.
- Желтуха новорождённых тяжелее и дольше протекает, если ребёнок унаследовал генотип *28/*28.
- Усиление симптомов при любых инфекционных и воспалительных состояниях: вирусные инфекции и другие нагрузки переводят субклинический Жильбер в явный с постоянной билирубиновой нагрузкой на ткани.
Причины заболевания
Синдром Жильбера относится к наследственным состояниям; при этом одного только генетического варианта недостаточно, чтобы синдром обязательно проявился.
Генетическая основа: необходимое, но недостаточное условие
Стандартная медицинская трактовка: синдром Жильбера — наследственное нарушение метаболизма билирубина, обусловленное мутациями в гене UGT1A1. Самый изученный вариант — UGT1A1*28 (семь TA-повторов в промоторе гена вместо шести), снижающий экспрессию фермента на 50–70%.
Но это только часть картины.
Во-первых, ген UGT1A1 — не изолированная единица. Он входит в большой комплекс UGT1A (гены 1A1–1A10), расположенный на хромосоме 2q37.1. Полиморфизмы в соседних генах, особенно UGT1A3, влияют на ферментную активность через явление генетического сцепления. Помимо *28, клинически значимы варианты *6, *7, *27, *37, *60, *63, *93 — всего более 100 патогенных вариантов. Стандартный лабораторный тест проверяет только один: *28. Это означает, что «отрицательный» генетический анализ не исключает синдром.
Во-вторых, и это принципиально важно: генетический вариант лишь задаёт сниженный «запас прочности» ферментной системы. Многие носители *28/*28 годами живут с нормальным или пограничным билирубином — пока не появляются внешние факторы, которые опрокидывают систему. Именно эти факторы и являются практической мишенью.
Триггеры: что запускает синдром
Согласно действующим клиническим рекомендациям (EASL, UpToDate, Российское общество по изучению печени), основными провоцирующими факторами при синдроме Жильбера являются:
- Голодание и низкокалорийные диеты — снижают захват билирубина гепатоцитами и усиливают «физиологический» гемолиз; провоцирующий эффект воспроизводится в клинических тестах (48 ч голодания → двукратный рост билирубина).
- Любые инфекции и интеркуррентные заболевания — за счёт воспалительного ответа и повышенной нагрузки на систему обезвреживания.
- Психоэмоциональный и физический стресс — через активацию гипоталамо-гипофизарно-надпочечниковой оси и изменение иммунного ответа.
- Нарушения сна и хроническое недосыпание — снижают иммунный контроль.
- Алкоголь — прямая гепатотоксичность.
- Ряд лекарственных препаратов — конкурентно ингибируют UGT1A1 или увеличивают нагрузку на печень.
- Менструация (у женщин) — за счёт циклического лёгкого гемолиза.
Герпесвирусы как триггер: взгляд превентивной медицины
Следующий раздел отражает клинический опыт и позицию врачей команды профессора Дадали — подход опирается на данные о биохимических механизмах, опубликованные клинические случаи и личный врачебный опыт.

«Синдром Жильбера проявляется из-за поражения клеток эндотелия капилляров герпесами».
– Лия Аркадьевна Алексеева, Врач общей практики, невролог, иммунолог с опытом работы более 30 лет.
Среди всех перечисленных триггеров особого внимания заслуживают хронические инфекции вирусами семейства герпеса. Их роль в провокации симптомов синдрома Жильбера недооценивается в стандартной практике — и вот почему это важно понимать.
Вирусы герпеса присутствуют в организме практически каждого взрослого человека. Носительство вируса Эпштейна–Барр (EBV, HHV-4) достигает 90–95% к 30 годам, цитомегаловируса (CMV, HHV-5) — 60–90%, HHV-6 — более 90%. В латентном состоянии они «молчат». Но при любом ослаблении иммунного контроля — стресс, недосыпание, голодание, лекарственная нагрузка, другая острая инфекция — происходит реактивация, и вирусы начинают активно воздействовать на ткани.
Почему именно через эндотелий?
Все перечисленные вирусы обладают тропизмом к эндотелиальным клеткам сосудов — в том числе к эндотелию синусоидов печени (liver sinusoidal endothelial cells, LSECs). Эти клетки выстилают мельчайшие капилляры-синусоиды, через которые вся кровь, идущая из кишечника, фильтруется через печень. LSECs — не просто «трубка»: они активно участвуют в регуляции воспаления, иммунного ответа и микроциркуляции печени.
Исследования подтверждают: CMV-антиген выявляется в эндотелиальных клетках печёночных синусоидов при хроническом гепатите; HHV-6 обнаруживается в 22% случаев острой печёночной недостаточности неустановленной этиологии; в экспериментальных моделях заражение синусоидальных эндотелиальных клеток цитомегаловирусом нарушает их функцию. Поражение эндотелия герпесвирусами задокументировано также при атеросклерозе, системных васкулитах и синдроме хронической усталости.
Теоретические механизмы усиления гипербилирубинемии при реактивации герпесвирусов:
- Нарушение микроциркуляции в печени. Поражённый эндотелий синусоидов теряет нормальные фенестры (поры), через которые билирубин поступает к гепатоцитам для конъюгации. Нарушается транспорт субстрата к ферменту.
- Прямое поражение гепатоцитов. EBV, CMV, HHV-6 могут вызывать вирусный гепатит с лимфоцитарной инфильтрацией и цитолизом гепатоцитов — клеток, где непосредственно работает UGT1A1. Описаны клинические случаи выраженной желтухи при EBV-гепатите у пациентов с синдромом Жильбера.
- Аутоиммунный гемолиз. При активном EBV у 40–60% пациентов образуются холодовые агглютинины, атакующие собственные эритроциты. Гемолиз в клетках ретикулоэндотелиальной системы резко увеличивает поток непрямого билирубина.
- Цитокиновое подавление транспортных белков. TNF-α, IL-1β, IL-6 — провоспалительные цитокины, высвобождаемые при реактивации герпесвирусов — подавляют транспортёры гепатоцитов (OATP1B1, MRP2), отвечающие за захват билирубина из крови и его экскрецию в желчь.
- Временное снижение экспрессии UGT1A1. Воспалительные цитокины могут эпигенетически регулировать транскрипцию UGT1A1, дополнительно снижая активность и без того ослабленного фермента.
Итог: у человека с генетически сниженной активностью UGT1A1 (синдром Жильбера) реактивация герпесвирусов одновременно увеличивает приток непрямого билирубина (гемолиз), нарушает его транспорт (поражение эндотелия синусоидов), снижает активность фермента ещё больше (цитокины, гепатоцитолиз) и блокирует экскрецию (нарушение желчетранспортных белков). Это и объясняет, почему именно после вирусных инфекций синдром Жильбера впервые «выходит» в анализах — или резко усиливается у тех, кто уже о нём знал.
Несмотря на отсутствие рандомизированных исследований по данной теме, понимание этих механизмов помогает объяснить, почему симптомы синдрома нередко усиливаются после болезней, стресса и других состояний, связанных с реактивацией латентных инфекций.
Симптомы
Большинство людей с синдромом Жильбера не имеют выраженных симптомов — или не связывают их с этим синдромом. Признаки синдрома Жильбера чаще всего появляются в периоды активации триггеров.
Наиболее частые проявления:
- Периодическая желтоватость склер и кожи (иктеричность) — главный видимый признак
- Общая усталость, снижение энергии — не всегда объясняемое внешними причинами
- Тяжесть или дискомфорт в правом подреберье
- Тошнота, снижение аппетита в период обострения
- Головные боли, раздражительность, снижение концентрации — особенно при высоком билирубине
Уровень билирубина при синдроме Жильбера обычно колеблется в диапазоне 1–5 мг/дл (17–85 мкмоль/л). Интенсивной желтухи с зудом, обесцвеченным стулом или тёмной мочой нет — эти симптомы требуют исключения другой патологии.
Важно: хроническое умеренное повышение непрямого билирубина — это не «просто цифры». У части пациентов оно сопровождается усталостью и когнитивными ощущениями («туман»). У взрослых с синдромом Жильбера периодически описываются когнитивные симптомы (затуманенность сознания, трудности с концентрацией), которые усиливаются именно в периоды подъёма билирубина.
Как синдром Жильбера проявляется у мужчин и женщин
У мужчин синдром дебютирует раньше (подростковый возраст), проявляется ярче, уровень билирубина в среднем выше. Голодание провоцирует подъём значительно сильнее, чем у женщин. Интенсивные физические нагрузки (марафон, HIIT) могут вызывать механический гемолиз эритроцитов → временный пик билирубина.
У женщин синдром протекает мягче, но имеет специфический «гормональный» паттерн: усиление желтушности во время менструации и в лютеиновой фазе цикла, при приёме оральных контрацептивов, при беременности. Принципиальных генетических различий нет — разница определяется гормональной средой.
Методы диагностики
Диагностика синдрома Жильбера строится прежде всего на клинической и биохимической картине. Генетический тест — лишь дополнительное подтверждение, и стандартный тест на UGT1A1*28 охватывает только один из более чем 100 возможных вариантов.
Лабораторная картина синдрома Жильбера:
| Показатель | При синдроме Жильбера |
| Общий билирубин | Повышен (1–5 мг/дл, иногда до 6) |
| Непрямой билирубин | >70–80% от общего |
| АЛТ, АСТ, ЩФ, ГГТ | Норма — обязательное условие |
| Общий анализ крови | Норма (гемолиза нет или минимален) |
| Гаптоглобин | Норма (снижение = признак значимого гемолиза) |
| УЗИ органов брюшной полости | Норма, без структурных изменений |
Золотое правило: изолированное повышение непрямого билирубина при нормальных показателях печёночных ферментов и отсутствии гемолиза — это синдром Жильбера до доказательства обратного.
Провокационные тесты (могут быть назначены при неясной картине):
Тест с голоданием (48 ч, 400 ккал/сутки): у людей с СЖ билирубин вырастает в 2 раза и более.
Тест с рифампицином (900 мг): специфичный подъём непрямого билирубина из-за конкурентного ингибирования транспорта.
Расширенный генетический анализ UGT1A1 (несколько вариантов): показан прежде всего перед химиотерапией иринотеканом или при планировании беременности.
Дифференциальная диагностика — исключить:
- Гемолитические анемии (снижен гаптоглобин, повышены ретикулоциты)
- Острые вирусные гепатиты (повышены АЛТ/АСТ)
- Синдром Криглера–Найяра (тяжёлая гипербилирубинемия >20 мг/дл)
- Синдромы Дубина–Джонсона и Ротора (преимущественно прямой билирубин)
Учитывая роль герпесвирусов как триггеров, имеет смысл обсудить с врачом оценку вирусной нагрузки (EBV, CMV, HHV-6), состояние иммунного статуса, маркёры воспаления (СРБ, ферритин, IL-6).
Лечение
Согласно действующим клиническим рекомендациям, синдром Жильбера не требует медикаментозного лечения. Основная задача в рамках официального ведения — исключить более серьёзную патологию, успокоить пациента и информировать его об известных лекарственных взаимодействиях.
Для ситуационного снижения билирубина применялся фенобарбитал (индуктор UGT1A1 через ядерный рецептор CAR) — сегодня крайне редко ввиду выраженных побочных эффектов. Других специфических препаратов нет.
Чего реально стоит опасаться: лекарственные взаимодействия
Это главный практический риск синдрома Жильбера у взрослых. Ряд препаратов метаболизируется именно ферментами UGT, и при сниженной активности UGT1A1 их концентрация в крови может нарастать до токсической.
Критически важно:
- Иринотекан (химиотерапия колоректального рака): его активный метаболит SN-38 инактивируется UGT1A1. При генотипе *28/*28 элиминация снижена на 61% → жизнеугрожающая нейтропения и диарея. FDA обязывает снижать стартовую дозу на 30%. Это медицинское противопоказание, а не рекомендация.
- Атазанавир и ряд других антиретровирусных препаратов (ВИЧ-терапия): ингибируют UGT1A1 напрямую → значимое нарастание желтухи у носителей *28/*28.
- Парацетамол при длительном регулярном применении: UGT1A1 участвует в его глюкуронизации; теоретически при хроническом приёме может снижаться инактивация токсичного метаболита NAPQI. Разовые терапевтические дозы при острой боли или температуре — допустимы, хронический ежедневный приём — требует консультации врача.
- Статины: у ряда пациентов с синдромом Жильбера описывается усиленное накопление лактонных метаболитов. При появлении мышечных болей на фоне статинотерапии — повод сообщить врачу и рассмотреть коррекцию дозы или смену препарата.
- Варфарин: возможны изменения фармакокинетики, требующие внимания при подборе дозы.
Работа с триггерами: реальная точка приложения усилий
Поскольку ген изменить невозможно, вся практическая работа — с модифицируемыми факторами.
- Вирусная нагрузка и иммунитет
Любые острые инфекции и реактивация хронических вирусных инфекций значительно усиливают проявления синдрома Жильбера — через воспаление, дополнительный гемолиз и нарушение функции печени. Поэтому при синдроме Жильбера особенно важно поддерживать нормальный иммунный ответ: восполнять установленные дефициты (витамин D, цинк, селен и др.), следить за качеством сна, не «обнулять» иммунный ответ жёсткими диетами и переутомлением. При признаках активной инфекции — обязательная консультация врача.
- Функция печени и нагрузка на детоксикацию
Поскольку у людей с синдромом Жильбера изначально снижена активность UGT1A1, задача — не перегружать печень лишними токсическими факторами. Практически это означает: регулярное питание без длительных голодных промежутков, достаточная гидратация, максимально возможное ограничение алкоголя и бессистемного приёма лекарств (особенно парацетамола, НПВС и других гепатотоксичных средств).
На этом фоне разумно обсуждать с нутрициологом гепатопротективные нутрицевтики (расторопша/силимарин, артишок, фосфолипиды) — они не противопоказаны при синдроме Жильбера. Миф об их запрете не имеет клинической базы: изменение фармакокинетики силимарина при *28/*28 не сопровождается токсичностью.
- Базовое нутриентное обеспечение
Ферментные системы детоксикации и антиоксидантной защиты зависят от того, достаточно ли в рационе белка, витаминов, минералов и незаменимых жирных кислот (включая омега‑3). Это и есть базовый уровень, без которого любые таргетированные добавки работают значительно слабее.
Уже на таком фундаменте, индивидуально и по рекомендации специалиста, могут подключаться дополнительные вещества, поддерживающие конъюгацию и антиоксидантную защиту: N‑ацетилцистеин (предшественник глутатиона), глицин и таурин (субстраты для конъюгации), а также отдельные антиоксиданты и полифенольные соединения. Прямых рандомизированных исследований именно при синдроме Жильбера для этих нутрицевтиков нет, поэтому их использование опирается на биохимические механизмы и всегда обсуждается индивидуально с врачом или нутрициологом.
Синдром Жильбера и защитный потенциал билирубина: парадокс
Умеренно повышенный непрямой билирубин при синдроме Жильбера обладает выраженными антиоксидантными и противовоспалительными свойствами и может защищать сосуды от избыточного окислительного стресса. В крупных наблюдательных исследованиях у людей с более высоким билирубином реже встречались сердечно‑сосудистые события и общая смертность была примерно на треть ниже, однако это отражает лишь статистическую связь, а не прямое «лечебное» действие билирубина.
Поэтому сегодня корректнее считать синдром Жильбера не фактором риска, а, скорее, нейтральной или условно благоприятной особенностью обмена, если билирубин повышен умеренно и стабильно. Насторожить должны не сами цифры, а нетипичные для СЖ ситуации — резкий рост билирубина, появление боли, зуда, тёмной мочи или обесцвеченного стула, когда важно искать другую причину, а не пытаться «нормализовать» билирубин любой ценой.
Часто задаваемые вопросы
1. Можно ли принимать расторопшу при синдроме Жильбера?
Да, можно. Миф о «запрете расторопши» не имеет клинического обоснования. Силимарин действительно метаболизируется ферментами UGT, и его фармакокинетика у носителей *28/*28 несколько меняется, но он не образует токсичных метаболитов и не вызывает гепатотоксичности. Антиоксидантные и гепатопротективные свойства расторопши при синдроме Жильбера — скорее плюс.
2. Можно ли заниматься спортом?
Да, регулярные нагрузки умеренной интенсивности полезны и не противопоказаны. Экстремальные нагрузки (марафон, интенсивные HIIT-сессии) могут провоцировать кратковременный механический гемолиз и подъём билирубина — эпизодический феномен без долгосрочных последствий. Голодание перед тренировкой — значительно вреднее, чем сама тренировка.
3. Нужна ли специальная диета?
Нет жёстких запретов. Жирная пища сама по себе не противопоказана. Ключевое правило: не голодать более 12–14 часов, питаться регулярно. Это одно из самых простых и эффективных практических действий при синдроме Жильбера.
4. Передаётся ли синдром детям?
Да, наследуется по аутосомно-рецессивному типу. Если оба родителя — носители *28, вероятность гомозиготного ребёнка (*28/*28) — 25%. Однако проявится ли синдром клинически — во многом зависит от совокупности внешних факторов в течение жизни ребёнка.
5. Синдром Жильбера и беременность — что нужно знать?
Беременность возможна и не противопоказана. Необходимо информировать акушера-гинеколога, контролировать уровень билирубина, особенно в третьем триместре. Повышен риск затяжной желтухи новорождённого, особенно при сочетании с другими факторами (ГВ, ABO-несовместимость, Г6ФД). Часть лекарств, применяемых в акушерстве, требует осторожности из-за метаболизма через UGT1A1.
Заключение
Синдром Жильбера — не «просто генетическая особенность», о которой можно забыть. Это состояние, при котором в организме существует хроническое слабое звено — сниженная активность фермента UGT1A1. Это слабое звено годами может никак себя не проявлять — до тех пор, пока не включаются триггеры.
С позиции доказательной медицины, ключевые триггеры — голодание, любые инфекции и воспалительные нагрузки, стресс, лекарства. С позиции превентивной медицины (так называемой «медицины здорового человека»), которой придерживается команда профессора Дадали, особого внимания заслуживает роль хронических герпесвирусных инфекций как систематически действующего фактора, усиливающего проявления синдрома через поражение эндотелия синусоидов печени и воспалительные механизмы.
В обоих подходах практический вывод один: перенести фокус с «у меня плохой ген» на «что из того, что нагружает мою ферментную систему, я могу контролировать» — качество иммунного ответа, режим питания и сна, осторожность с лекарствами.
Источники
- Синдром Жильбера: благоприятные, неблагоприятные и противоречивые аспекты. A.P. De Silva et al. World J Hepatol., 2025, 17(2), 98503. PubMed, ID 40027563
- Взаимодействие распространённых путей метаболизма лекарственных средств и меры предосторожности при их применении у пациентов с синдромом Жильбера. D.C. Dacheng et al. Zhonghua Gan Zang Bing Za Zhi., 2025, 33(3), 293–299. PubMed, ID 40274556
- Острая печёночная недостаточность и вирус HHV-6: реактивация при иммунопарезе. I.M. Correia et al. GE Port J Gastroenterol., 2024, 32(4), 293–299. PubMed, ID 40726553
- Инфицирование синусоидальных эндотелиальных клеток печени мышиным цитомегаловирусом (Muromegalovirus muridbeta1): участие нейропилина-1 и зависимость от динамин-опосредованного эндоцитоза. I. Kyrrestad et al. Front Cell Infect Microbiol., 2023, 13, 1249894. PubMed, ID 38029264
- Инфекция эндотелиальных клеток герпесвирусами как системная патогенетическая ось при миалгическом энцефаломиелите/синдроме хронической усталости. J.M. Nunes et al. Viruses, 2024, 16(4), 572. PubMed, ID 38675914
- Вирус герпеса человека 6 типа и острая печёночная недостаточность. M. Härmä et al. Transplantation, 2003, 76(3), 536–539. PubMed, ID 12923440
- Гепатит, ассоциированный с вирусом Эпштейна–Барр, у подростка без типичных симптомов инфекционного мононуклеоза на фоне синдрома Жильбера: клиническое наблюдение. R.L. Dennis 3rd et al. Cureus, 2024, 16(10), e71925. PubMed, ID 39564031
- Желтуха как редкое проявление первичной инфекции вирусом Эпштейна–Барр. L.R. Santos et al. Cureus, 2021, 13(6), e15609. PubMed, ID 34277228
- Совокупное влияние регуляторных полиморфизмов на транскрипцию UGT1A1 как причина синдрома Жильбера. K. Matsui et al. BMC Gastroenterol., 2010, 10, 57. PubMed, ID 20529348
- Гипербилирубинемия, улучшение функции эндотелия и снижение окислительного стресса при синдроме Жильбера. T. Maruhashi et al. Circulation, 2012, 126(5), 598–603. PubMed, ID 22773454
- Синдром Жильбера и риск смерти: популяционное когортное исследование. L.J. Horsfall et al. J Gastroenterol Hepatol., 2013, 28(10), 1643–1647. PubMed, ID 23701650
- Билирубин и эндотелиальная функция. T. Maruhashi et al. J Atheroscler Thromb., 2019, 26(8), 688–696. PubMed, ID 31270300
- Роль уридиндифосфат-глюкуронозилтрансферазы 1A1 (UGT1A1) в метаболизме и фармакокинетике флавонолигнанов силимарина у пациентов с хроническим гепатитом C и неалкогольной жировой болезнью печени. Y. Xie et al. Molecules, 2017, 22(1), 142. PubMed, ID 28098838